Nernst方程和Goldman方程的主要区别在于,能斯特方程描述了还原电位与标准电极电位之间的关系,而Goldman方程是能斯特方程的导数,描述了细胞膜上的反转电位。
电化学电池是利用化学反应的化学能发电的电气装置。或者,我们可以用这些装置通过提供所需的电能来辅助化学反应。电化学电池的还原电位决定了电池产生电的能力。
目录
1. 概述和主要区别
2. 什么是能斯特方程
3. 什么是高盛方程
4. 并列比较——能斯特方程与高盛方程的表格形式
5. 摘要
什么是能斯特方程(nernst equation)?
能斯特方程是一个数学表达式,它给出了电化学电池的还原电位和标准还原电位之间的关系。这个方程是以科学家沃尔特·能斯特的名字命名的。此外,还利用了其他影响电化学氧化还原反应的因素,如温度和氧化还原化学物质的化学活性。
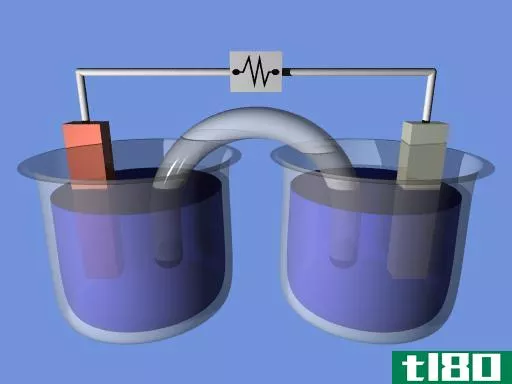
在推导能斯特方程时,我们必须考虑吉布斯自由能的标准变化,这种变化与电池中发生的电化学转变有关。电化学电池的还原反应如下:
Ox+z e–⟶红色
根据热力学,反应的实际自由能变化是,
E=还原-氧化
但是,吉布斯自由能(ΔG)与E(势差)有关,如下所示:
ΔG=-nFE
式中,n是反应进行时化学物质之间转移的电子数,F是法拉第常数。如果考虑标准条件,则方程如下:
ΔG0=-nFE0
我们可以通过下面的方程把非标准条件的吉布斯自由能和标准条件的吉布斯能联系起来。
ΔG=ΔG0+RTlnQ
然后将上述方程代入标准方程,得到能斯特方程如下:
-nFE=-nFE0+RTlnQ

然而,我们可以用法拉第常数和R(普适气体常数)的值重写上述方程。
E=E0–(0.0592VlnQ/n)
什么是高盛方程(goldman equation)?
在细胞膜生理学中,Goldman方程在确定跨细胞膜的反向电位时很有用。这个方程是以科学家大卫·E·戈德曼的名字命名的,他开发了这个方程。它是从能斯特方程推导出来的。Goldman方程考虑了离子在细胞膜上的不均匀分布和膜通透性的差异。公式如下:
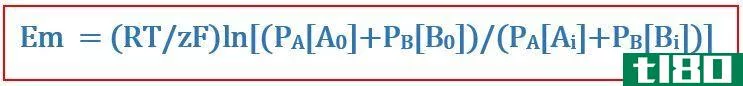
在哪里?
- Em是细胞膜上的电位差,
- R是宇宙气体常数,
- T是热力学温度,
- Z是在化学物质之间转移的电子的摩尔数,
- F是法拉第常数,
- PA或B是膜对A或B离子的渗透性,以及
- [A或B]i是A或B离子在细胞膜内的浓度。
能斯特方程(nernst equation)和高盛方程(goldman equation)的区别
Nernst方程和Goldman方程是一种数学表达式,可作为电化学电池电位的测量。Nernst方程与Goldman方程的关键区别在于,Nernst方程描述了还原电位与标准电极电位之间的关系,而Goldman方程是Nernst方程的一个导数,描述了细胞膜上的反转势。
下面的信息图总结了能斯特方程和高盛方程之间的区别。

总结 - 能斯特方程(nernst equation) vs. 高盛方程(goldman equation)
Nernst方程和Goldman方程是可以用来测量电化学电池电位的数学表达式。Nernst方程和Goldman方程的关键区别在于,Nernst方程描述了还原电位与标准电极电位之间的关系,而Goldman方程则是能斯特方程的导数,描述了细胞膜上的反转电位。
引用
1“能斯特方程”,化学剧本,剧本,2019年6月5日,可在这里查阅。