4楼(4f)和5f轨道(5f orbitals)的区别
主要区别4f(main difference 4f) vs. 5f轨道(5f orbitals)
原子是由质子和中子组成的原子核,质子和中子被电子包围。这些电子在原子核周围连续运动。因此,我们不能给出电子在原子中的具**置。科学家们引入了“概率”的概念,而不是确定电子的确切位置。换句话说,确定了电子最有可能运动的最可能路径。这个路径叫做轨道。有不同的轨道子集,如s轨道、p轨道、d轨道和f轨道。每个子集中的轨道数由磁量子数决定。对于f轨道,有7个可能的磁量子数,所以有7个f轨道。4f和5f轨道是f轨道的第一组和第二组。4f和5f轨道的主要区别是4f轨道有许多平面和圆锥节点,但没有径向节点,而5f轨道有许多平面和圆锥节点,每个轨道有一个径向节点。
覆盖的关键领域
1.什么是4f轨道-定义,七个轨道及其相对相似性2.什么是5f轨道-定义,七个轨道及其相对相似性3.4f和5f轨道之间的相似性是什么-共同特征概述4.4f和5f轨道之间的差异是什么-主要差异的比较
关键词:原子,电子,波瓣,磁量子数,节点,核,轨道,概率,子壳层

什么是4f轨道(4f orbitals)?
4f轨道是第四电子壳层的七个f轨道(能级)。4f轨道是f轨道的第一个子集。这意味着第一,第二和第三电子壳层没有f轨道。这在下面的s,p,d和f轨道表中显示。
| 电子壳层 | 轨道 |
| 1 | s |
| 2 | s、 第 |
| 三 | s、 p、d |
| 4 | s、 p、d、f |
| 5 | s、 p、d、f |
一组4f轨道有四种不同的形状,每种形状都有许多平面和圆锥形节点。但是4f轨道没有径向节点。这七个4f轨道是根据轨道的平面来命名的。下面给出了7个4f轨道。
- 4fxyz公司
- 4fz3型
- 4fz(x2-y2)
- 4财年(3)×2-2年)
- 4fx(x2-3y2)
- 4fxz2型
- 4fyz2型
在这些轨道中,4fxyz和4fz(x2-y2)轨道都有八个波瓣。它们通过围绕z轴旋转45度而相互关联。这意味着,它们在其他因素上是相似的,但在平面上是不同的。
在其余的七个轨道中,4fy(3×2-y2)和4fx(x2-3y2)轨道通过绕z轴旋转90°而相互关联。每个轨道有六个叶,由三个节面隔开,节面之间的夹角为60°。4fxz2和4fyz2轨道似乎与4fy(3)相似×2-y2)和4fx(x2-3y2)轨道不同,因为六个平面的三个节面没有60°角分开。这些4fxz2和4fyz2轨道在z轴上有两个“豆形”的六个波瓣。另一方面,4fxz2轨道与4fxz2和4fyz2轨道的轨道相似,但“豆形”波瓣位于x轴上。在4fyz2轨道中,“豆形”轨道位于y轴。
什么是5f轨道(5f orbitals)?
5f轨道是第五电子壳层的七个f轨道(能级)。5f轨道是f轨道的第二个子集。这些轨道是根据轨道平面命名的。七个轨道如下。
- 5fxyz型
- 5fz3型
- 5fz(x2-y2)
- 5财年(3)×2-2年)
- 5fx(x2-3y2)
- 5fxz2型
- 5fyz2型

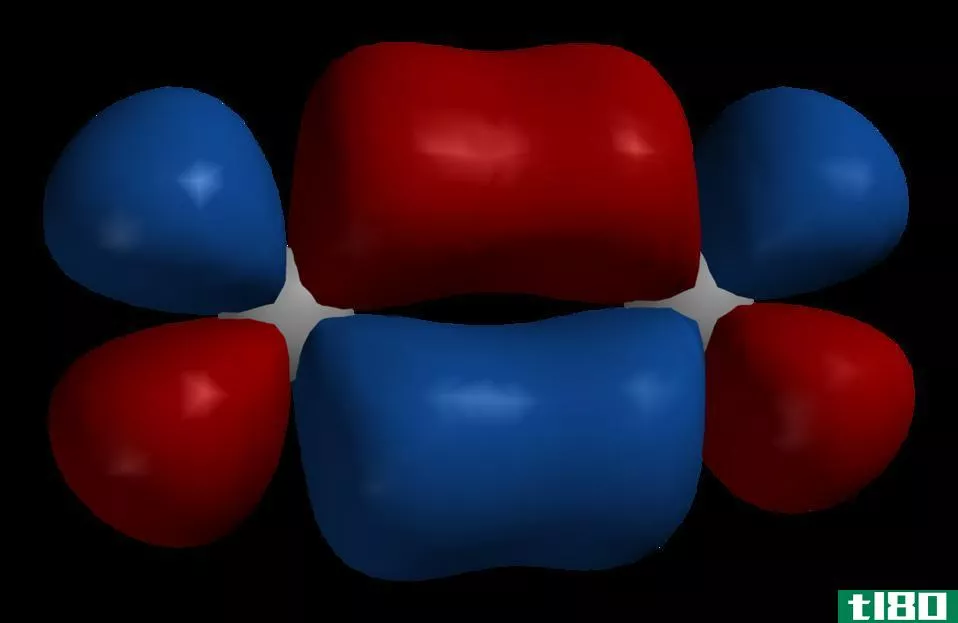
Figure 1: Seven Different f Orbitals
一组5f轨道有四种不同的形状,每种形状都有许多平面和圆锥形节点。每个5f轨道也有一个径向节点。
在这些轨道中,5fxyz和5fz(x2-y2)轨道都有八个波瓣。它们通过围绕z轴旋转45度而相互关联。这意味着,它们在其他因素上相似,但在所指向的平面上不同。
在其余的七个轨道中,5fy(3×2-y2)和5fx(x2-3y2)轨道通过绕z轴旋转90°而相互关联。每个轨道有六个叶,由三个节面隔开,节面之间的夹角为60°。5fxz2和5fyz2轨道与5fy(3)轨道相似×2-y2)和5fx(x2-3y2)轨道,但它们是不同的,因为六个平面的三个节面没有60度角分开。这些5fxz2和5fyz2轨道也有六个“豆形”波瓣中的两个。另一方面,5fxz2轨道与5fxz2和5fyz2轨道的轨道相似,但“豆形”的波瓣在x轴上。在5fyz2轨道中,“豆形”轨道位于y轴。
4f和5f轨道的相似性
- 两者都是f轨道形式。
- 两者在同一平面上有相似的形状。
- 两者都有复杂的轨道结构。
4楼(4f)和5f轨道(5f orbitals)的区别
定义
4f轨道:4f轨道是第四电子壳层的七个f轨道(能级)。
5f轨道:5f轨道是第五电子壳层的七个f轨道(能级)。
子集
4f轨道:4f轨道是f轨道的第一个子集。
5f轨道:5f轨道是f轨道的第二个子集。
放射状节点
4f轨道:4f轨道有许多平面和锥形节点,但没有径向节点。
5f轨道:5f轨道有许多平面和圆锥节点,每个5f轨道也有一个径向节点。
大小
4f轨道:4f轨道比5f轨道小。
5f轨道:5f轨道比4f轨道大。
结论
原子在其电子壳层中由不同形式的轨道组成:s轨道、p轨道、d轨道和f轨道。f轨道的加入是从第四电子壳层(能级)开始的。4f和5f轨道的主要区别是4f轨道有许多平面和圆锥节点,但没有径向节点,而5f轨道有许多平面和圆锥节点,每个轨道也有一个径向节点。
引用
1.马克J温特。”原子轨道:4f(总集)。“轨道子:原子轨道和分子轨道画廊,2015年7月12日,可在这里获得。2。马克J温特。”原子轨道:5f(常规设置)。“轨道子:原子轨道和分子轨道画廊,2015年7月12日,可在这里获得。 2.马克J温特。”原子轨道:5f(总集)。“轨道子:原子轨道和分子轨道画廊,2015年7月12日,
- 发表于 2021-06-30 00:20
- 阅读 ( 612 )
- 分类:科学
你可能感兴趣的文章
自旋轨道耦合(spin-orbit coupling)和拉塞尔桑德斯效应(russell-saunders effect)的区别
自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。 分析化学中的耦合主要是指轨道和电子...
- 发布于 2020-09-29 23:05
- 阅读 ( 520 )
轨道图(orbital diagram)和电子组态(electron configuration)的区别
轨道图和电子构型的关键区别在于,轨道图用箭头表示电子,表示电子的自旋。但是,电子组态没有显示电子自旋的细节。 轨道图显示了由电子组态给出的电子排列。电子组态给出了电子在整个原子轨道上分布的细节。但是...
- 发布于 2020-10-14 00:32
- 阅读 ( 737 )
px py公司(px py)和pz轨道(pz orbitals)的区别
Px-Py和Pz轨道的关键区别在于Px轨道有两个沿x轴方向的波瓣,Py轨道有两个沿y轴方向的波瓣,而Pz轨道有两个沿z轴方向的波瓣。因此,Px-Py和Pz轨道之间的差异源于它们在空间中的取向。 An atomic orbital is a region around an atomic nucleu...
- 发布于 2020-10-14 02:27
- 阅读 ( 943 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。 有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论...
- 发布于 2020-10-15 22:50
- 阅读 ( 842 )
反键合(antibonding)和非键合(nonbonding)的区别
反键和非键的关键区别在于反键轨道增加了分子的能量,而非键轨道不会改变分子的能量。 反键和非键这两个术语都属于分子轨道理论。根据这个理论,这些轨道是由于其他轨道重叠而形成的混合轨道。 目录 1. 概述和主要...
- 发布于 2020-10-16 03:12
- 阅读 ( 1268 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
混合轨道和退化轨道的关键区别在于,混合轨道是两个或多个轨道混合形成的新轨道,而退化轨道最初存在于原子中。 正如它的名字所暗示的,混合轨道是两个或更多轨道的混合。虽然简并轨道的名称看起来是一样的,但它...
- 发布于 2020-10-16 17:47
- 阅读 ( 899 )
镧系收缩(lanthanide contraction)和锕系收缩(actinide contraction)的区别
...的原子半径和离子半径都在不断减小。此外,这是因为4f轨道在填满5d轨道之前充满了电子。在这里,4f电子对核电荷的屏蔽性很差,这反过来又导致6s电子向原子核移动,导致半径变小。 图01:周期表 此外,这种收缩是很有规律...
- 发布于 2020-10-16 20:20
- 阅读 ( 906 )
纯净的(pure)和杂化轨道(hybrid orbitals)的区别
纯轨道和杂化轨道的关键区别在于,纯轨道是原始原子轨道,而杂化轨道是由两个或多个原子轨道混合而成。 在简单分子的化学键形成过程中,我们可以简单地考虑原子轨道的重叠。但是如果我们要讨论复杂分子中的化学键...
- 发布于 2020-10-17 13:43
- 阅读 ( 559 )
vbt公司(vbt)和cft公司(cft)的区别
...描述原子间不同化学键形成的理论。这个理论解释了原子轨道的重叠或混合形成化学键。CFT一词代表晶体场理论。它是一个用来解释电子轨道(通常是d或f轨道)的简并(等能量电子壳层)由于周围阴离子或阴离子(或配体)产...
- 发布于 2020-10-19 11:35
- 阅读 ( 465 )
轨道(orbit)和轨道(orbital)的区别
轨道与轨道的关键区别在于,轨道是一条围绕中心点有固定路径的环形路径,而轨道是围绕原子核的不确定区域。 虽然术语“轨道”和“轨道”听起来相似,但这是两个不同的术语。轨道一词主要与行星有关,而轨道一词则...
- 发布于 2020-10-23 03:43
- 阅读 ( 450 )